
|
Nauka » Biologia » Biologia molekularna Przyszłość komórek macierzystych w medycynie [1] I would like to thank Dr. Jonas
Frisen from Karolinska Institute in Stockholm
for his courtesy and for granting me permission to reproduce the figures
from his articles. This article would not be ever written without his and his
colleagues' magnificent work on adult stem cells research. W świecie nauki toczy się gorąca debata nad szerokim zastosowaniem embrionalnych komórek macierzystych (ESC — ang. Embryonic Stem Cells) w terapiach przyszłości. Komórki macierzyste pobrane z rozwijającego się tworu embrionalnego odznaczają się niesamowitą wręcz plastycznością — potrafią nabyć specjalizację, czyli przekonwertować się w każdy specyficzny rodzaj tkanki organizmu, np. w komórki skóry, komórki kościotwórcze, kurczliwe komórki mięśniowe, czy komórki nerwowe. W miarę rozwoju organizmu komórki budujące nasze tkanki tracą tę plastyczność pozostając przy swojej funkcji. W tkankach wymagających regeneracji, odbudowy i produkcji nadal posiadamy dorosłe komórki macierzyste (ASC — ang. Adult Stem Cells), jednak o ograniczonej plastyczności — komórki szpiku przekształcają się głównie w komórki dynamicznej struktury kości oraz w komórki krwi. Komórki w hipokampie, bardzo ważnej części naszego mózgu, dają początek funkcjonalnym komórkom nerwowym. Posiadamy również komórki dające początek naszej warstwie skórnej, czy tkance śluzowo-receptorowej w komorze nosowej. Dorosłe komórki macierzyste są wyspecjalizowane w produkcji konkretnych tkanek i posiadają naturalne blokady, dzięki którym nie rozwijają się niekontrolowanie. Chroni nas to nie tylko przed wyrośnięciem niepotrzebnych organów, ale przed niebezpiecznymi procesami różnicowania, które mogą doprowadzić do rozwoju nowotworu. Ostatnie badania wykazują jednak, że dorosłe komórki macierzyste posiadają niespodziewanie duży potencjał do przekształcania się w obce im tkanki i mogą mieć duże zastosowanie w inżynierii tkankowej oraz terapii przewlekłych chorób.  Rycina 1. Embrionalna komórka macierzysta — wielka i jednocześnie kontrowersyjna nadzieja medycyny. Przyszłość pokaże, czy naukowcy będą w stanie odnaleźć alternatywę. (Dzięki uprzejmości H.Orkin [1]) Problem początku człowiekaWspomniana na początku debata ma podłoże przede wszystkim etyczne — wielu ludzi uważa — bazując na religii, czy też intuicyjnym poczuciu, — że rozwijający się embrion jest od samego powstania istotą ludzką, gdyż początek jej istnienia to poczęcie. Argumentacja taka paradoksalnie wypada na korzyść klonowania terapeutycznego — stadium blastocysty, od której pobiera się komórki macierzyste nie powstaje bynajmniej poprzez proces poczęcia, czyli połączenia plemnika z komórką jajową. (patrz Ryc.2) 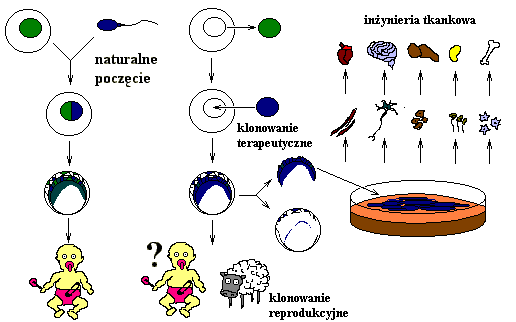 Rycina 2. Schematyczne porównanie naturalnego poczęcia (po lewej) oraz otrzymanie zarodka na drodze klonowania. Klonowanie terapeutyczne i reprodukcyjne mają taki sam początek — usunięcie materiału genetycznego dawczyni komórki jajowej i wprowadzenie obcego DNA. Dziesięciodniowy zarodek posiada obszar zawierający komórki macierzyste do pobrania. Na obecnym etapie nie jesteśmy pewni, czy klonowanie reprodukcyjne działa u ludzi. Rozdzielenie komórek macierzystych od reszty zarodka pozwala na ich namnożenie na pożywce i poprzez odpowiednią stymulację na transformację w pożądany typ komórek. W uproszczeniu, od dawczyni pobierana jest komórka jajowa, z której usuwa się materiał genetyczny (który w przypadku poczęcia naturalnego połączyłby się z materiałem plemnikowym). Następnie pobiera się cały materiał genetyczny od dawcy z jednej z jego komórek i wstrzykuje się do wydrążonej komórki jajowej. Impuls elektryczny pobudza komórkę do dalszych podziałów i tworzenia zarodka. Specyficzny obszar z tworu embrionalnego posiada komórki macierzyste, które można wyodrębnić i wysiać na pożywkę. Osobiście jestem zwolennikiem powszechnego w nauce poglądu, iż embrion staje się człowiekiem w momencie wykształcenia układu nerwowego i zdolności do wszelkich przejawów odczuwania. Nazywanie zlepka kilku komórek człowiekiem jest pewnym nieporozumieniem. Jestem raczej skłonny do nazywania omawianego stadium potencjalnym człowiekiem, który np. wskutek złego zagnieżdżenia się w ścianie macicy nigdy się nim nie stanie. Poza tym nie jesteśmy nawet pewni, czy możliwe jest uzyskanie człowieka techniką klonowania, chociażby bazując na niedawnych doniesieniach o niezbędności plemnika w utworzeniu zdrowego embrionu. Wyodrębnienie komórek macierzystych z wczesnego stadium embrionalnego nie jest zatem „zabijaniem", bo po pierwsze nie zaistniało poczęcie, po drugie szanse na rozwinięcie w płód są znikome. Czas pokaże, czy naukowcy znajdą alternatywę do badań nad embrionalnymi komórkami macierzystymi. Science factionAby uzmysłowić sobie zastosowanie praktyczne ESC przenieśmy się w przyszłość i pozwól, drogi Czytelniku, że popuszczę tu trochę wodze fantazji, opartej jednakże na solidnych podstawach naukowych. Właśnie dowiadujemy się, że na skutek pewnych pochorobowych powikłań nasze nerki przestały pracować. Z trwogą wspominamy dawne czasy, kiedy należało przechodzić męczącą dializę co trzy dni i bezskutecznie oczekiwać latami na przeszczep, licząc jednocześnie na czyjąś tragiczną śmierć. Otrzymując nerkę, istniało również ryzyko odrzutu, powikłań, nie wspominając o efektach ubocznych brania leków immunosupresyjnych przez resztę życia. Po krótkiej konsultacji z lekarzem i niezbędnych badaniach pobierany jest nasz materiał genetyczny, który zostaje wstrzyknięty do wydrążonych komórek jajowych dawczyń. Po selekcji z jednego z rozwijających się na pożywce zarodków pobrana zostaje warstwa komórek macierzystych, które zostają namnożone w hodowli. Ich wystarczająca ilość zostaje wysiana na silikonowy szkielet, w którym są odpowiednio rozlokowane substancje dające sygnał komórkom macierzystym o kierunku przemian. Tak stymulowane mogą zamieniać się w tkankę korową nerki, czy naczynia krwionośne. Hodowana nerka niekoniecznie idealnie przypomina „oryginalną" — musi spełniać jedynie wyznaczoną dla niej funkcję, czyli filtrować krew z odpadowych substancji metabolicznych. Może być np. mniejsza, co ułatwia jej umieszczenie bez usuwania starych nerek, aby uniknąć komplikacji. Nadchodzi dzień zabiegu chirurgicznego, podczas którego otrzymujemy w prezencie nic innego jak naszą własną nerkę! Brak ryzyka odrzutu, brak potrzeby brania wyniszczających leków hamujących odporność organizmu. Powoli dochodzimy do siebie po zabiegu i dowiadujemy się, że nasz stary znajomy również przechodzi rekonwalescencje w tym samym szpitalu. Miał duże szczęście — kilka tygodni temu spadł z galopującego konia i miał pęknięty kręgosłup w kilku miejscach. Wkrótce po wypadku, lekarze bazując na klonowaniu terapeutycznym wstrzyknęli mu zróżnicowane embrionalne komórki macierzyste w miejsca urazu i właśnie wraca mu czucie i potrafi powoli poruszać wszystkimi kończynami. Czyż medycyna przyszłości nie zaczyna przypominać jeszcze niedawno nieprawdopodobnych powieści science-fiction? Dalsza część artykułu pokaże, że już obecne dokonania często powodują zawroty głowy — opisywana w mojej „historyjce" technika już dzisiaj ma swoje początki — inżynierowie prowadzą zaawansowane badania nad tzw. drukowaniem narządów (ang. Organ Printing), gdzie w specjalnych hydrożelach formuje się warstwy sztucznych narządów wypełnionych komórkami, które już potrafią formować rurkowate twory będące idealnym podłożem dla formowania systemu krwionośnego.[2] Inżynierowie tkankowi we współpracy z embriologami będą w stanie w przyszłości podać nam naszą dodatkową wątrobę na tacy... Postęp w nauce a etykaPowróćmy na jednak na Ziemię i do naszego czasu. Nie uważam bynajmniej, że nauka powinna być zupełnie pozbawiona pewnych ograniczeń etycznych. Ma ona służyć dobru ludzkości, nie zaś wykolejonym zachciankom przestępców, pozbawionym jakichkolwiek skrupułów. Jednak w przypadku komórek macierzystych zakaz prowadzenia badań nad ESC może poważnie ograniczyć postęp i zniweczyć szansę wielu chorych, którzy mogliby zostać wyleczeni z kalectwa, uciążliwej choroby czy uratowani przed powolną śmiercią. Ostatnio jednak, pozytywnie dla obu stron, pojawiają się coraz bardziej obiecujące sygnały o zaskakującym potencjale dorosłych komórek macierzystych. Może i intensywne badania nad ASC staną się nadzieją nowoczesnej inżynierii tkankowej i leczenia urazów takich jak przerwany rdzeń kręgowy czy uszkodzone serce po zawale. Batalia o komórki macierzyste rozciągnęła się na wszystkie płaszczyzny życia, sprzeczne donosy powodują zagubienie nie tylko samych naukowców, ale przede wszystkim społeczeństw i ludzi sprawujących władzę. Dlatego poszczególne państwa miotają się pomiędzy przysłowiowym młotem a kowadłem. Osobiście uważam za bardzo słuszne wprowadzenie jednogłośnego zakazu klonowania reprodukcyjnego, które również uważam, przynajmniej na razie, za nieetyczne. Kwestia klonowania terapeutycznego podzieliła świat i końcowe decyzje o zakazie badań nad komórkami embrionalnymi zostały przełożone na rok 2005 [3] a szczegółowe kwestie zostały powierzone poszczególnym państwom UN. Jak na razie Stany Zjednoczone korzystają z jedynie 12 już istniejących dostępnych linii ESC, a naukowcy nie są upoważnieni do tworzenia nowych hodowli. Wielka Brytania i Szwecja są jak na razie najbardziej radykalnymi państwami, które zalegalizowały klonowanie terapeutyczne.[4] Ach, te wspaniałe embrionalne komórki macierzystePrzewaga ESC nad ASC jest przygniatająca. Embrionalne komórki macierzyste posiadają niewiarygodną plastyczność, do eksperymentalnych terapii podawać je można już zróżnicowane lub formie pierwotnej, w zależności od doświadczenia. Aby uzmysłowić sobie ich potencjał podam przykład doświadczenia. Ludzkie embrionalne komórki poddano różnicowaniu w komórki nerwowe. Następnie transplantowano je w kręgosłupy sparaliżowanych szczurów z uszkodzonym rdzeniem, które po pewnym czasie były ponownie zdolne do chodzenia! [5] Mało tego, inny zespół naukowców powtórzył ten eksperyment z niezróżnicowanymi ludzkimi ESC. I w tym przypadku, szczury z uprzednio poprzerywanymi rdzeniami kręgowymi odzyskiwały zdolność do czucia i poruszania się.[5] Wstrzyknięte komórki macierzyste były zdolne do odzyskania starych szlaków nerwowych oraz do tworzenia nowych neuronów. Przykład ten jest imponujący również dlatego, że ESC były zdolne do pobudzenia regeneracji u innego gatunku! Czy opowiedziana przeze mnie futurystyczna historyjka o znajomym z urazami kręgosłupa po upadku z siodła nadal wydaje się nieprawdopodobna? Z powodu poważnych restrykcji dotyczących doświadczeń na ludziach pierwsze próby kliniczne będą miały miejsce dopiero za mniej więcej półtora roku.
« Biologia molekularna (Publikacja: 12-06-2004 Ostatnia zmiana: 19-06-2004)
str. 3443 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [ Regulamin publikacji ] [ Bannery ] [ Mapa portalu ] [ Reklama ] [ Sklep ] [ Zarejestruj się ] [ Kontakt ] Racjonalista © Copyright 2000-2018 (e-mail: redakcja | administrator) | ||





 Ukończył biologię molekularną na Uniwersytecie Adama Mickiewicza w Poznaniu. Pracował jako Research Specialist in Health Science w Department of Anatomy and Cell Biology na University of Illinois w Chicago. Obecnie pracuje jako Associate Cell Biologist / Histologist w Abbott Laboratories (Illinois). Specjalizuje się w ekspresji białek 'od zera', hodowlach linii komórkowych, symulacji in vitro procesów zachodzących w komórkach. Jego pasją jest teoria ewolucji, w szczególności ewolucja systemów biochemicznych i pochodzenie życia we Wszechświecie.
Ukończył biologię molekularną na Uniwersytecie Adama Mickiewicza w Poznaniu. Pracował jako Research Specialist in Health Science w Department of Anatomy and Cell Biology na University of Illinois w Chicago. Obecnie pracuje jako Associate Cell Biologist / Histologist w Abbott Laboratories (Illinois). Specjalizuje się w ekspresji białek 'od zera', hodowlach linii komórkowych, symulacji in vitro procesów zachodzących w komórkach. Jego pasją jest teoria ewolucji, w szczególności ewolucja systemów biochemicznych i pochodzenie życia we Wszechświecie.